Forfattere
Aksonerne i vores nerver er som lange ledninger, der bærer vigtige kommunikationssignaler rundt i kroppen. Aksonerne er ikke alene i nerverne; de er omgivet af særlige celler kaldet Schwann-celler. Dette følgeskab gør det muligt for vores kroppe at gøre ting som at gå i skole, gribe en bold og spise. Hos nogle mennesker med sygdomme, der kaldes neuromuskulære sygdomme, bliver aksonerne alvorligt syge og kan visne væk. Vi opdagede, at når axoner bliver syge, opdager Schwann-cellerne hurtigt problemet. Schwann-cellerne fungerer som et nødberedskab, der leverer en ekstra forsyning af specielle sukkerstoffer til aksoner i nød. Denne sukker-boost gør de skadede aksoner stærkere og giver dem mulighed for at komme sig. Vi håber, at denne opdagelse vil føre til nye terapier, der vil hjælpe med at holde axoner i live hos syge mennesker.
Alle, der har set Paw Patrol, ved, at denne canadiske tv-tegnefilm handler om kommunikation og teamwork for at hjælpe venner og naboer i problemer. Ligesom i Paw Patrol fungerer cellerne i vores kroppe som et team. De kombinerer deres kræfter for at gøre det muligt for os at udføre alle vores daglige aktiviteter, såvel som at vokse og reparere skader på vores kroppe. En legendarisk fysiolog, Theodor Schwann, beskrev engang vigtigheden af dette cellulære kammeratskab. Han skrev: “Hele organismen eksisterer kun ved hjælp af de enkelte elementære deles gensidige påvirkning” [1].
Hvad sker der, hvis en del af dette system bliver sygt og ikke fungerer godt? Når celler eller væv bliver syge, bliver det cellulære teamwork stærkere. Med andre ord tilkalder celler med problemer hjælp fra andre celler. Disse celler arbejder så sammen om at løse problemet. Hjælpen kan ske gennem udveksling af næringsstoffer eller brændstoffer, der er nødvendige for at opretholde cellernes energimetabolisme.
Energimetabolisme er den proces i alle vores celler, der nedbryder mad for at producere energi gennem kemiske reaktioner. Energimetabolismen er absolut nødvendig for livet. Hvad nu, hvis der ikke er nok brændstof til rådighed i en celletype? Ville det så stoppe cellens stofskifte? Nej, for andre celler griber ind og overfører nye brændstoffer. Et tydeligt eksempel på dette teamwork opstår under intens træning eller sult [2]. Desperate celler i hjertet, hjernen eller musklerne kalder på hjælp fra leveren. Levercellerne frigiver så særlige nødbrændstoffer, som transporteres gennem blodet for at nå de organer og celler, der har brug for det.
Aksoner er fingerlignende forlængelser af neuroner (nerveceller) i vores nervesystem. For tydeligt at kunne observere aksoner i laboratoriet kan neuroner fjernes fra nervesystemet og overføres til en særlig skål med en barriere (figur 1). Denne barriere gør det muligt at adskille de neuronale cellelegemer og axonerne. Aksonerne kan derefter studeres i detaljer gennem et mikroskop. Forskere bruger dette system som en simpel model til at simulere neuronernes opførsel i nervesystemet.
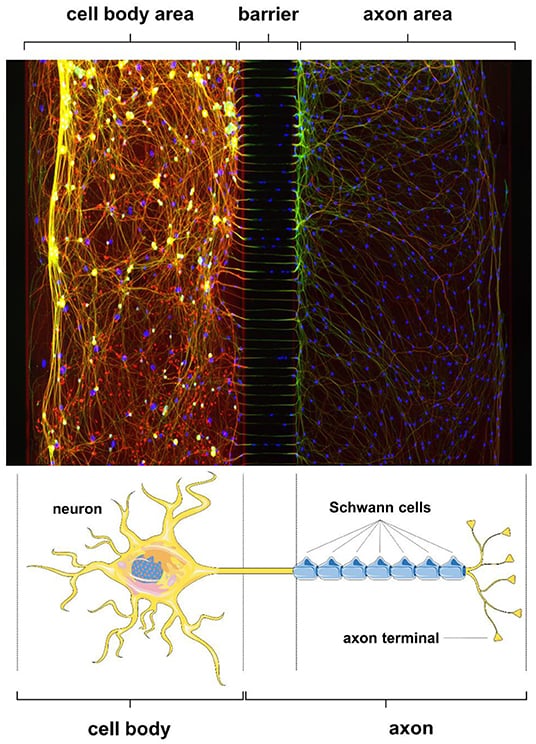
I vores kroppe forbindes axonet fra en neuron typisk med en anden neuron eller celletype. Denne forbindelse gør det muligt for axonet at tale med en anden neuron eller celle. De kommunikerer ved hjælp af et sprog lavet af elektriske og kemiske signaler. For eksempel taler aksoner med muskel- og sanseceller, hvilket gør det muligt for os at bevæge os og føle.
Men billederne i figur 1 viser, at aksoner faktisk er meget tyndere og længere end fingre. Vidste du, at aksoner med deres spidser (aksonterminaler, figur 1 nederst, højre, figur 2B) udgør den største del af neuronet [3]? I menneskekroppen kan aksoner være op til en meter lange! Hvis du forestiller dig, at neuronets cellekrop er på størrelse med en tennisbold, ville axonet være mange kilometer langt! For at holde sig i live og sunde skal aksonerne modtage vigtige materialer fra neuronernes cellekrop. Processen med at transportere materialer langs aksoner er blevet beskrevet i en tidligere Frontiers for Young Minds-artikel [4]. Da transporten af disse materialer langs aksoner kan være en meget lang rejse, bruger den meget energi. Det gælder især for de lange aksoner i nervesystemet uden for hjernen og rygmarven, som kaldes det perifere nervesystem (PNS). Nerver er som lange kabler, der bærer bundter af aksoner tæt pakket sammen (figur 2A). Sådanne særligt lange aksoner i nerver kan meget let knække.
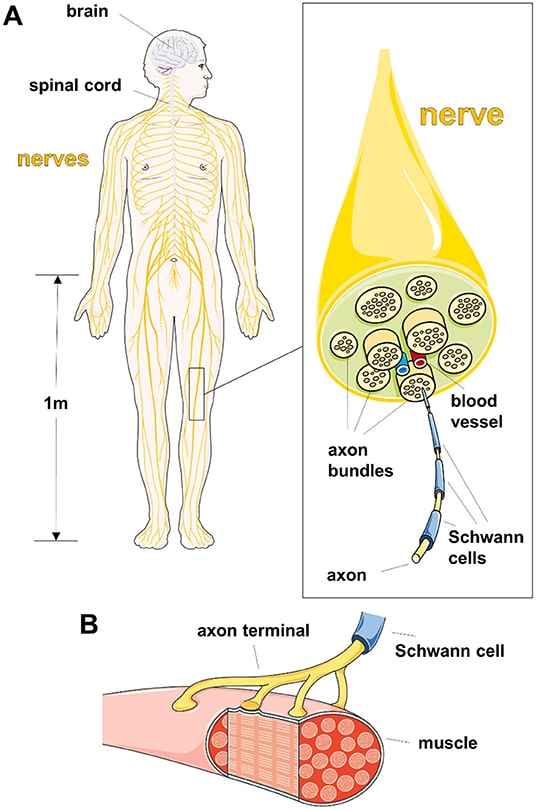
Naturen har designet unikke celler, kaldet Schwann-celler (opkaldt efter førnævnte Theodor Schwann, der opdagede dem), som støtter axoner på forskellige måder. Schwann-cellerne omfavner aksonerne for at beskytte dem (figur 1, 2). Denne tætte kontakt nærer og styrker axonerne i nerverne i PNS. Schwann-celler kan levere vigtige næringsstoffer til axonerne, hvilket er meget hurtigere for axonerne end at få næringsstoffer fra den neuronale cellekrop, der ligger langt væk. Typisk er der mange tusinde Schwann-celler forbundet med hvert axon, hvilket skaber et vigtigt makkersystem.
Som enhver spinkel og skrøbelig struktur knækker aksoner først, når tingene går galt. Hvad sker der, hvis aksonerne forringes? Husk, at mange neuroner er forbundet med hinanden i serier via deres aksoner. Selv hvis kun ét akson i kæden knækker, kan den normale informationsstrøm langs nerven blive forstyrret.
Forskning i laboratoriet og på patienter har vist, at aksoner beskadiges tidligt i mange sygdomme i nervesystemet. Dette spænder fra Alzheimers og Parkinsons sygdom og traumatiske hjerneskader [5], til neuromuskulære sygdomme som motorneuronsygdom og perifere neuropatier[6]. Perifere neuropatier kan påvirke armenes og benenes bevægelser ved at ødelægge de aksoner, der forbinder dem med musklerne. De afkoblede muskler bliver svage, slappe og skrumper til sidst med tiden. Nogle gange bliver vejrtrækningen vanskelig, og hjerteslaget svækkes, fordi de aksoner, der forbinder lungerne og hjertemusklerne, degenererer.
Det er nogle af de værste sygdomme, man kan få, og på nuværende tidspunkt findes der ingen kur mod dem. Forskere rundt om i verden på universiteter og medicinalfirmaer arbejder hårdt på at forstå, hvorfor og hvordan axoner dør. Med denne viden forsøger de at finde måder at forsinke eller forhindre degenerationen af aksoner på. En nylig undersøgelse har vist, at faldet i energi i skadede aksoner forklarer, hvorfor de til sidst falder fra hinanden [7]. Vi spurgte: “Er det muligt at beskytte skadede aksoner ved at tilføre energi udefra neuronet?” Hvis ja, spurgte vi derefter: “Kunne Schwann-celler levere denne energi til skadede aksoner?” Vi stillede også disse spørgsmål, fordi vi var inspireret af det generelle princip om metabolisk brændstofudveksling mellem forskellige celler og det cellulære teamwork, der blev beskrevet i indledningen. Vi var desuden motiveret af vores tidligere opdagelse af, at forstyrrelse af energimetabolismen i Schwann-celler forårsager axon-degeneration [8].
Ved hjælp af en række forskellige metoder og neurovidenskabelige modeller opdagede vi, at Schwann-celler faktisk kommer til undsætning!
Vi fandt ud af, at skadede aksoner udvikler en øget appetit på visse specielle sukkermolekyler kaldet pyruvat og laktat. Når de fornemmer skadede aksoner, producerer Schwann-celler større mængder pyruvat og laktat gennem en proces, der kaldes glycolysis Sukkerstofferne optages derefter af skadede aksoner som brændstof til at producere energi i deres mitokondrier for at fremme axonal genopretning (figur 3). Med andre ord bliver Schwann-cellerne en slags energisk nødstøttesystem for skadede aksoner. Vi mener, at dette er en naturlig måde at hjælpe seks aksoner med at overleve på. Naturlige skader på aksoner opstår for eksempel, når nerverne bevæger sig i vores lemmer, eller når vi ældes.
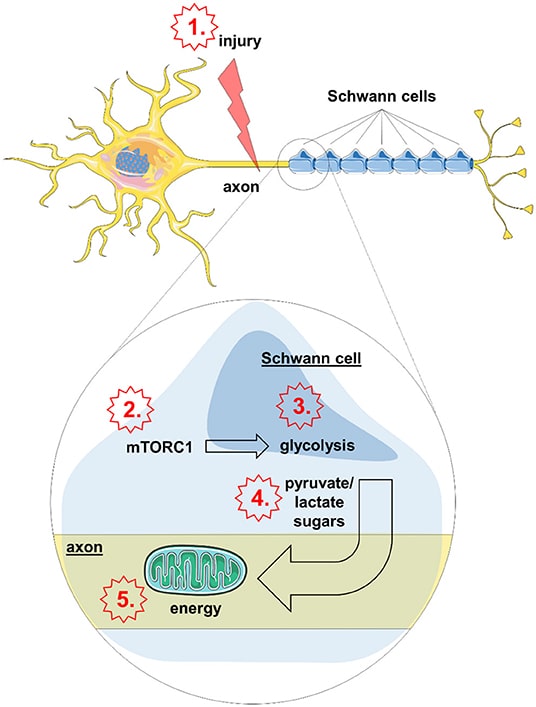
Hvad vil der ske, hvis vi ændrer selve glykolysen i Schwann-cellerne? Hvad med hvis vi ændrer frigivelsen af sukker fra Schwann-cellerne? Vi fandt ud af, at degenerationen af skadede aksoner fremskyndes eller bremses i sådanne situationer. Vi identificerede også, hvad der får Schwann-cellerne til at ændre deres glykolyse. Det er et lille, men mægtigt molekylært signal fra en stor proteinkrop kendt som mTORC1 (mammalian target of rapamycin complex 1). Kan vi så ændre aktiviteten af dette signal, så det beskytter axoner ved sygdom? For at teste dette gjorde vi aksoner i laboratoriemus syge med et giftigt stof kendt som akrylamid. Dette stof forårsager aksonsygdom i menneskelige nerver. Vi tvang Schwann-cellerne til at producere mere sukker ved at øge mTORC1-signalet over længere tid. Det havde en beroligende effekt på aksoner, der var blevet såret af akrylamid. På denne måde var det for første gang muligt at beskytte skadede aksoner uden for neuronet.
Vi ved nu, at skadede aksoner i nerver degenererer på grund af problemer med at få nok energi. Aksoner danner unikke relationer med Schwann-celler. Det tætte bånd mellem axoner og Schwann-celler støtter axonerne. Vi har fundet en måde at beskytte syge aksoner på gennem øget tilførsel af energi i form af sukkerstoffer, der frigives fra Schwann-cellerne. Det er spændende at have fundet en celletype, der kontrollerer axonernes sundhed på denne interessante måde. I mange år har forskerne fokuseret på at beskytte aksonerne primært gennem behandling af selve neuronet. Nu har vi viden om endnu en mekanisme til at forbedre axonernes sundhed!
Hvordan kan vores resultater bruges til at hjælpe menneskelige patienter? I fremtiden kan denne viden anvendes til at bekæmpe tab af axoner hos patienter med sygdomme i nervesystemet. Det kan være muligt at øge glykolysen og sukkerfrigivelsen fra menneskelige Schwann-celler for at hjælpe axonerne med at komme sig efter skader. Eller måske kan vi give de axonbeskyttende sukkerstoffer direkte til patienterne for at lindre deres symptomer. Det vil også være interessant at se, om lignende mekanismer beskytter axoner i hjernen og rygmarven, ud over axoner i nerver. De celler, der omgiver sådanne aksoner, er kendt som oligodendrocytter og astrocytter Opretholder disse celler sammen aksoner ved også at levere sukkerstoffer (ligesom Schwann-celler)? Der er stadig meget, der skal undersøges for i sidste ende at hjælpe patienter med sygdomme, hvor axon-degeneration spiller en nøglerolle. Men vi har et stærkt håb om, at ingen axon er for lang, og ingen Schwann-celle er for lille til at redde dagen for mange syge mennesker!
Det perifere nervesystem: Den del af nervesystemet, der ligger uden for hjernen og rygmarven.
Alzheimers sygdom: En neurodegenerativ sygdom med hævelse og degeneration af aksoner i hjernen, der forårsager dårlig hukommelse og tænkning.
Parkinsons sygdom: En neurodegenerativ sygdom med degeneration af axoner i mellemhjernen, der resulterer i rystelser og stivhed i lemmerne.
Multipel sklerose: En neurodegenerativ sygdom i hjernen og rygmarven, hvor aksonfibre degenererer på grund af uhensigtsmæssige immunangreb.
Perifere neuropatier: En stor gruppe af neurodegenerative sygdomme i det perifere nervesystem, hvor nerveaksoner degenererer af forskellige årsager.
Glykolyse: En central metabolisk vej, der nedbryder sukkermolekylet glukose for at producere to af et mindre sukkermolekyle kaldet pyruvat. Pyruvat kan derefter omdannes til laktat.
Mitokondrier: Organeller i vores celler, som producerer det meste af den energi, der driver cellernes biokemiske reaktioner.
mTORC1 (mammalian Target of Rapamycin Complex 1): En central signalinstruktør i alle vores celler, som kontrollerer metabolisme og vækst.
Oligodendrocytter: Celler med lignende funktioner som Schwann-celler i det perifere nervesystem. Oligodendrocytter omgiver direkte axoner i hjernen og rygmarven.
Astrocytter: Stjerneformede celler i centralnervesystemet, der er tæt forbundet med neuroner for at levere næringsstoffer og regulere overførslen af elektriske signaler.
[1] Schwann, T., og Smith, H. 1847. Cellernes teori, mikroskopiske undersøgelser af overensstemmelsen i dyrs og planters struktur og vækst. London: Sydenham Society.
[2] Cantrell, C. B., og Mohiuddin, S. S. 2020. Biokemi, ketonmetabolisme. Treasure Island, FL: StatPearls.
[3] Beirowski, B. 2013. Koncepter til regulering af aksonintegritet ved indpakning af glia. Front. Cell. Neurosci. 7:256. doi: 10.3389/fncel.2013.00256
[4] Sleigh, J. 2020. Axonal transport: leveringssystemet, der holder nerveceller i live. Forsiden. Young Minds. 8:12. doi: 10.3389/frym.2020.00012
[5] ↑ Morrow, E. L., og Duff, M. C. 2020. Hvordan er restitution efter traumatisk hjerneskade? Forside. Young Minds. 8:559017. doi: 10.3389/frym.2020.559017
[6] Coleman, M. P., og Perry, V. H. 2002. Axonpatologi i neurologisk sygdom: et forsømt terapeutisk mål. Trends Neurosci. 25:532-7. doi: 10.1016/s0166-2236(02)02255-5
[7] Yang, J., Wu, Z., Renier, N., Simon, D. J., Uryu, K., Park, D. S., et al. 2015. Patologisk aksonal død gennem en MAPK-kaskade, der udløser et lokalt energiunderskud. Cell. 160:161-76. doi: 10.1016/j.cell.2014.11.053
[8] Beirowski, B., Babetto, E., Golden, J. P., Chen, Y. J., Yang, K., Gross, R. W., et al. 2014. Metabolisk regulator LKB1 er afgørende for Schwann-celle-medieret axonvedligeholdelse. Nat. Neurosci. 17:1351-61. doi: 10.1038/nn.3809
Mennesker har lavet musik i titusinder af år. Men hvad sker der i din hjerne, når du lytter til dit yndlingsband eller din yndlingsmusiker? I denne artikel følger du lydens rejse fra ørerne til hjernen, hvor forskellige områder arbejder sammen, mens du lytter til musik. Musik involverer mange hjernefunktioner, såsom lydbehandling, hukommelse, følelser og bevægelse. Du vil også opdage, at hjernen kan lære at genkende velkendte mønstre i musik, hvilket kan hjælpe med at forklare, hvorfor musik kan gøre os glade, triste eller endda ophidsede. Til sidst vil du udforske, hvad der sker i musikeres hjerner, når de spiller på deres instrumenter.
…Kunstig intelligens (AI) systemer bliver ofte rost for deres imponerende præstationer inden for en lang række opgaver. Men mange af disse succeser skjuler et fælles problem: AI tager ofte genveje. I stedet for virkelig at lære, hvordan man udfører en opgave, bemærker den måske bare enkle mønstre i de eksempler, den har fået. For eksempel kan en AI, der er trænet til at genkende dyr på fotos, stole på baggrunden i stedet for selve dyret. Nogle gange kan disse genveje føre til alvorlige fejl, såsom en diagnose fr , der er baseret på hospitalsmærker i stedet for patientdata. Disse fejl opstår selv i avancerede systemer, der er trænet på millioner af eksempler. At forstå, hvordan og hvorfor AI tager genveje, kan hjælpe forskere med at designe bedre træningsmetoder og undgå skjulte fejl. For at gøre AI mere sikker og pålidelig skal vi hjælpe den med at udvikle en reel forståelse af opgaven – ikke bare gætte ud fra mønstre, der har fungeret tidligere.
…Er du nogensinde faldet og slået hovedet, mens du legede? Følte du dig lidt svimmel og havde ondt i hovedet? Hvis ja, kan du have fået en hjernerystelse! Hjernerystelser kan ske hvor som helst. De kan ske under sport, når du leger med dine venner eller endda når du cykler med dine forældre. Det kan være svært at vide, om du har fået en hjernerystelse. Mange børn og forældre er ikke sikre på, hvad de skal gøre, hvis nogen får en hjernerystelse. Læger og forskere ved, at det hjælper dig med at komme dig hurtigere, hvis du gør det rigtige efter en hjernerystelse. Denne artikel forklarer, hvad en hjernerystelse er. Den hjælper dig med at se, om du eller en ven har fået en hjernerystelse, og fortæller dig, hvad du skal gøre, hvis du nogensinde får en hjernerystelse.
…Hjertet er en meget vigtig muskel, der arbejder uafbrudt for at pumpe blod og levere vigtige næringsstoffer og ilt til alle dele af kroppen. Denne artikel ser på, hvordan hjertet fungerer normalt, og hvad der sker, når det fungerer unormalt, som det er tilfældet med en tilstand kaldet atrieflimren (AF). AF er en almindelig tilstand, der opstår, når hjertet slår uregelmæssigt og ude af takt. AF kan øge en persons risiko for at udvikle alvorlige problemer som hjertesvigt eller slagtilfælde. Denne artikel ser også på, hvordan AF kan diagnosticeres, hvad der forårsager AF, og de forskellige måder, det kan behandles på.
…