Forfattere
Aksoner er de tynde og lange forlængelser af neuronale celler, der slynger sig væk fra cellekroppen. Aksoner i vores nervesystem er som broer, der spænder over lange afstande for at bringe information fra en nervecelle til en anden. Men aksoner er levende og har brug for næringsstoffer og energi for at overleve. Aksoner degenererer, hvis de løber tør for næringsstoffer og energi. Det resulterer i ødelæggende symptomer i mange tilstande, der kaldes neurodegenerative sygdomme. Forskerne skal forstå, hvorfor og hvordan aksoner degenererer for at forhindre eller forsinke det. Nylige undersøgelser har identificeret en ødelæggelsesproces, der fører til energitab og død af skadede aksoner. Destruktionsprocessen afsluttes af et “nedrivningshold”, der drives af vagthundsmolekylet SARM1. Blokering af dette nedrivningshold forsinker døden af skadede aksoner og hjælper syge aksoner. Disse resultater kan føre til nye behandlingsformer, der kan mindske symptomerne hos mange mennesker, der lider af neurodegenerative sygdomme.
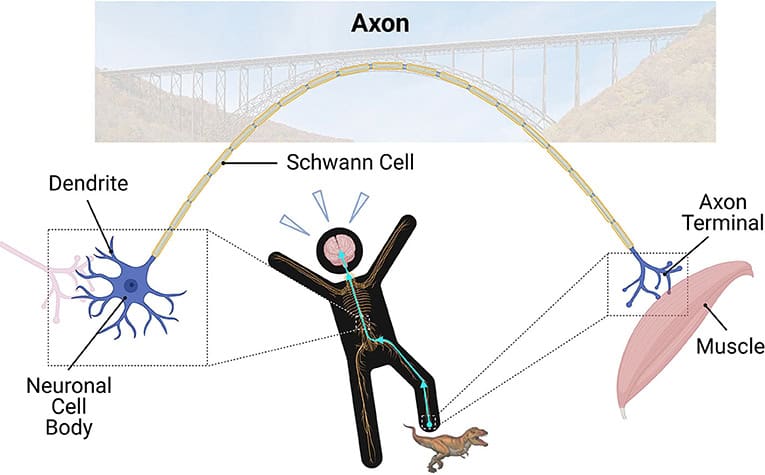
Det er tid til aftensmad, og du hører din mor kalde dig ud i køkkenet. Du springer op af sofaen, da din fod pludselig – YOW! – lander lige på en af din lillebrors dinosaurlegetøj med pigge! Du er måske ikke klar over det, men i løbet af den korte tid er der sendt utallige beskeder til din krop om, at den skal bevæge benene, trække foden væk og desværre føle smerten (figur 1).
Nervesystemet, som består af hjernen, rygmarven og en masse nerver, har ansvaret for at sende disse beskeder. Nervesystemet arbejder hele tiden, uden at vi er klar over det. Hver gang du griber en bold, mærker den bløde pels på en hund eller tager en matematiktest, er dit nervesystem på arbejde! Hjernen gør det muligt for os at lære og tænke. Rygmarven og nerver sender beskeder fra hjernen til kroppen og sender information til hjernen fra omverdenen.
Hvordan klarer vores nervesystem alle disse fantastiske ting? Særlige celler kaldet nerveceller eller neuroner kommunikerer information til resten af nervesystemet ved hjælp af kemiske og elektriske signaler.
Neuroner har fire hoveddele: dendritter, cellelegeme, akson og aksonterminalen (figur 1). Dendritter er de små grene af neuronen, der modtager indgående beskeder fra andre neuroner, som de er forbundet med. Signalerne bevæger sig derefter gennem neuronets cellelegeme, som er kontrolcentret for cellens aktiviteter. Til sidst når signalerne frem til den største del af neuronet: aksonet. Axoner strækker sig langt ud fra cellelegemet og videresender beskederne til andre neuroner eller mål. Det sker for enden af aksonet, som kaldes aksonterminalen. Ligesom broer gør det muligt for biler at køre og nå land på den anden side, er aksoner vigtige “broer” i nervesystemet (figur 1). De gør det muligt for elektriske og kemiske signaler at bevæge sig op til 1 m (3 fod) væk! Ingen anden celletype i din krop kan gøre det!
Større aksoner er dækket af en myelinskede. Det holder det elektriske signal stærkt og giver det et hastighedsboost. Myelinskederne er som isoleringen af elektriske kabler i væggene i dit hus. I nerverne hjælper særlige celler kaldet Schwann-celler med at lave myelinskederne (figur 1). I hjernen og rygmarven produceres myelinskederne af celler, der kaldes oligodendrocytter. Aksoner, der er samlet i bundter omgivet af myelin, ser hvide ud, når de undersøges i mikroskopet. Derfor kalder vi områder med disse strukturer for “hvid substans”.
Nogle gange går det galt i neuroner. Da aksoner er lange, tynde og følsomme strukturer, er de typisk de første, der går i stykker. Aksoner er også meget “sultne”. De har brug for masser af energi for at holde den elektriske og kemiske “trafik” flydende. Nyere studier har opdaget, at noget af den energi, som aksoner har brug for, kommer fra de omkringliggende Schwann-celler og oligodendrocytter.
Når der ikke er nok energi, kan trafikken langs aksonerne blive påvirket. Dette bidrager til aksondød. Som tidligere forklaret er aksoner vigtige for korrekt kommunikation mellem neuroner. Hvis for mange aksoner går til grunde, kan det forstyrre kommunikationen mellem neuronerne. Forestil dig, at flere basketballspillere på samme hold blev skadet på én gang. Det ville være meget svært for resten af holdet at spille godt! På samme måde kan aksondegeneration forstyrre holdet af neuroner.
Faktisk er aksondegeneration en tidlig og central begivenhed i mange neurodegenerative sygdomme. For eksempel er degeneration af aksoner, der forbinder musklerne (figur 1), en årsag til amyotrofisk lateral sklerose (ALS). Det fører til meget svage muskler, som gør det svært for patienterne at bevæge sig og trække vejret. Et andet eksempel er Alzheimers sygdom, hvor vigtige hjerneaksoner og deres terminaler degenererer. Det resulterer i problemer med hukommelse og tænkning. Ved øjensygdommen glaukom dør aksoner i synsnerven bag øjeæblet. Det kan medføre blindhed. Multipel sklerose er en anden sygdom, der giver mange ødelæggende symptomer. Vi er ikke sikre på hvorfor, men kroppens immunsystem angriber fejlagtigt myeliniserede aksoner i denne tilstand. I øjeblikket studerer hjerneforskere aksondegeneration for at forsøge at finde en måde at reducere den på. På den måde håber de at kunne hjælpe mennesker, der lever med neurodegenerative sygdomme.
Lad os tænke på axonet som en lang bro igen. Hvis der sker alvorlig skade på et akson, bliver “broen” svag, og den elektriske og kemiske “trafik” kan ikke længere køre sikkert over den. Et hærgende nedrivningshold slippes derefter løs for at rive broen ned, fordi det efter kroppens mening er bedre at rive en svært beskadiget bro ned end at forsøge at vedligeholde en ødelagt bro.
Den proces, hvor kroppen ødelægger den beskadigede del af et akson, kaldes Wallersk degeneration (Figur 2). Den britiske forsker Augustus Waller beskrev første gang denne proces, da han kiggede på afskårne frønerver gennem et mikroskop [1]. Kan du forestille dig, hvor svært det må have været med den teknologi, der fandtes for 170 år siden? På trods af dette fandt Augustus Waller ud af, at skadede aksoner i den overskårne frønerve går i stykker i en hurtig degenerationsproces. Andre celler end neuroner hjælper med at skille aksonerne ad.
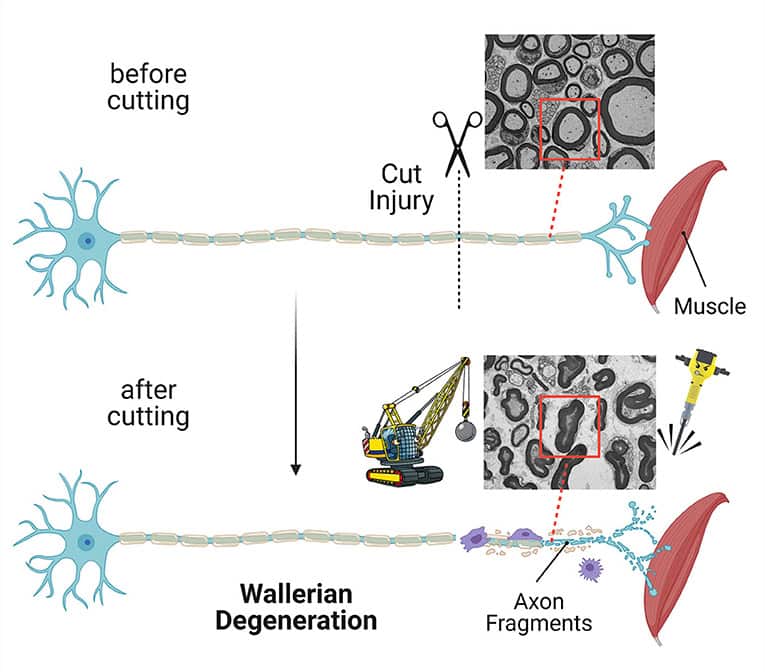
I laboratoriemus er ødelæggelsesprocessen færdig for tusindvis af afbrudte aksoner i en overskåret nerve inden for 2-3 dage efter skaden [2]. Det går endnu hurtigere, hvis vi kun ser på enkelte aksoner. De ødelægges hurtigt inden for få timer [2]. Se, det er hurtigt og rasende! Tænk på Wallersk degeneration som et ekspresnedrivningsprogram – i stedet for at lade broen smuldre og forfalde over tid, bruger nedrivningsholdet deres værktøjer til hurtigt at rive broen ned. Bagefter kommer et oprydningshold og fjerner resterne af aksonerne. Det hjælper med at bygge nye aksoner.
Ligner Wallersk degeneration den aksondegeneration, der sker ved neurodegenerative sygdomme? I de sidste tre årtier har neuroforskere fundet ud af, at aksondegenerationen i nerverne hos syge patienter i et mikroskop ligner Wallersk degeneration. Det er derfor, de kalder aksondøden i neurodegenerative sygdomme for Wallerian-lignende degeneration, selv om der ikke er tale om overskæring af aksoner. Derudover opdagede de, at særlige genetiske mutationer der blokerer nedrivningsprogrammet i mus, undertrykker i høj grad både Wallersk degeneration og Wallersk-lignende degeneration [3]. Forestil dig aksoner, der er adskilt fra deres cellelegemer, og som kan overleve i ugevis i de overskårne nerver hos mutante mus. De samme mutationer forsinker også degenerationen af syge aksoner og reducerer i nogle tilfælde symptomerne på neurodegenerative sygdomme. Det er også interessant, at de samme mutationer forårsager de samme effekter hos andre arter, f.eks. bananfluen. Det fortæller os, at ødelæggelsen af aksoner hos forskellige arter styres af det samme nedrivningsprogram. Det er vigtigt, at disse resultater viser, at en overskåret nerve kan bruges som en nyttig model til at forstå Wallerian-lignende degeneration i neurodegenerative sygdomme.
Selv om du måske foretrækker at spise slik, minder dine forældre dig om at spise frugt og grøntsager, fordi disse fødevarer indeholder vigtige næringsstoffer, der giver os energi og hjælper os med at holde os stærke. For at aksoner kan forblive stærke og sunde, har de brug for et særligt næringsstofmolekyle kaldet NAD. NAD spiller en vigtig rolle i axonets evne til at producere den energi, det har brug for til at overleve. Energien genereres gennem vejene glykolyse og mitokondrieånding som kræver NAD for at fungere. NAD fremstilles af molekylet NMN af enzymet NMNAT2. NMNAT2 distribueres gennem det sunde akson af et leveringssystem, der kaldes aksonal transport [4] (figur 3A). Når niveauet af NMNAT2 falder, fordi et akson er skadet eller sygt, kæmper aksonet på grund af det resulterende fald i NAD og energi (figur 3B).
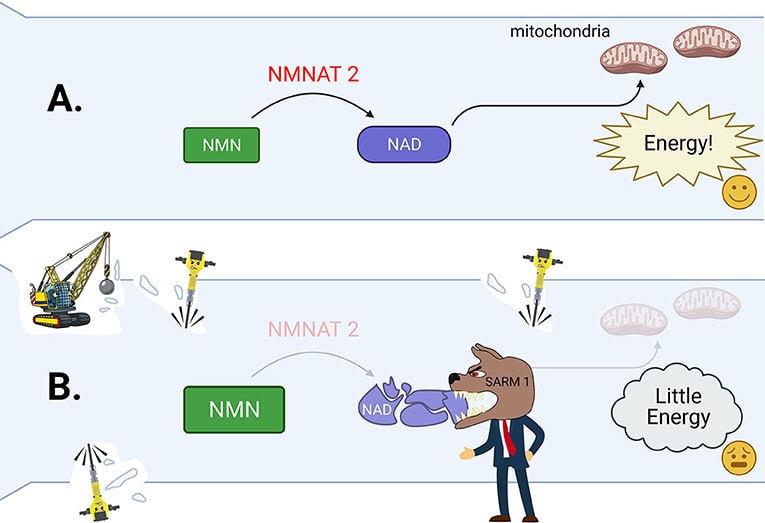
Men hvad sker der, hvis disse problemer tager overhånd? Kraftige ændringer af NMN og NAD udløser aktivering af molekylet SARM1 [5, 6]. SARM1 kan ses som en vagthund og chefen for det wallerske degenerationsnedrivningshold (figur 3B). Det holder konstant øje med, hvad der sker i aksonet ved at opsnuse mængderne af NAD og NMN. Når det aktiveres, ødelægger SARM1 al resterende NAD og fremskynder aksonets energitab. Det er nedrivningsholdets signal til at begynde at arbejde. Calpains er nedrivningsholdets vigtigste redskaber til at adskille syge aksoner. Disse værktøjer er enzymer, der hugger axonets stillads op som små jackhamre (figur 3).
For at vende tilbage til lighederne mellem wallersk og wallersk-lignende degeneration: Mange neuroforskere mener nu, at aktiveringen af SARM1 og nedrivningsholdet også finder sted i syge aksoner, i lighed med hvad der sker i afskårne aksoner. De mener, at blokering af SARM1 kan bruges til at redde aksoner i neurodegenerative sygdomme.
Aksoner kan let bryde sammen som smuldrende broer. Ødelæggelsen af aksoner ved Wallersk degeneration kan føre til alvorlige problemer i mange neurodegenerative sygdomme. Med vores nye viden om, hvordan nedrivningsholdet og deres kommandant kan kontrolleres, begynder vi at tro på, at der er måder, hvorpå vi kan redde aksoner. Måske vil læsere som jer en dag bruge jeres nervesystemer til at opdage nye måder at redde aksoner på, som kan hjælpe mennesker med mange neurodegenerative sygdomme!
Vi er taknemmelige for støtten til forskning på bachelorniveau på University at Buffalo gennem Experiential Learning Network (ELN)-programmet. Det nuværende arbejde i vores laboratorium er støttet af bevillinger fra National Institute of Health (R01NS111024, R01NS123450 og S10OD030488) og Muscular Dystrophy Association (577844) samt opstartsfinansiering fra Empire State Development Corporation for Hunter James Kelly Research Institute grant nos. W753 og U446 og Hunter’s Hope Foundation. Figurerne blev skabt ved hjælp af BioRender (https://biorender.com).
Neuro-degenerative sygdomme: En stor gruppe af sygdomme, der skyldes en gradvis nedbrydning af nervesystemet.
Wallersk degeneration: Den biologiske proces, hvor en afbrudt nervestump med dens skadede aksoner degenererer.
Mutation: En ændring i strukturen af et gen, som overføres til efterfølgende generationer og kan føre til produktion af et ændret protein.
NAD: Nikotinamid-adenin-dinukleotid: Molekyle, der findes i alle levende celler, og som er vigtigt for at forsyne cellerne med energi.
Glykolyse og mitokondriel respiration: Centrale stofskifteveje, der bruger sukkermolekylerne glukose og pyruvat til at producere energi.
Mitokondrier: Mitokondrier er specialiserede strukturer i vores celler, der er afgørende for energiproduktionen. Ligesom batterier driver de forskellige funktioner i cellerne.
NMN: Nicotinamid mononuculeotid: et molekyle, der bruges til at generere NAD.
Enzym: En klasse af proteiner, der skabes af alle organismer, og som er ansvarlige for at fremskynde biokemiske reaktioner.
NMNAT2: Nicotinamid mononukleotid adenylytransferase 2: Et enzym i aksoner, der hjælper med at producere NAD.
[1] Waller, A. 1850. Eksperimenter på sektionen af glossopharyngeal og hypoglossal nerver af frøen og observationer uf de alternativer, der produceres derved i strukturen af deres primitive fibre. Philos. Trans. R. Soc. Lond. B Biol. Sci. 140:423-9.
[2] Beirowski, B., Adalbert, R., Wagner, D., Grumme, D. S., Addicks, K., Ribchester, R. R., et al. 2005. Den progressive karakter af Wallersk degeneration i vildtype- og langsom Wallersk degeneration (WldS)-nerver. BMC Neurosci. 6:6. doi: 10.1186/1471-2202-6-6
[3] Coleman, M. P., og Hoke, A. 2020. Programmeret aksondegeneration: fra mus til mekanisme til medicin. Nat. Rev. Neurosci. (2020) 21:183-96. doi: 10.1038/s41583-020-0269-3
[4] Sleigh, J. N. 2020. Axonal transport: leveringssystemet, der holder nervecellerne i live. Front. Young Minds (2020) 8:2. doi: 10.3389/frym.2020.00012
[5] Figley, M. D., Gu, W., Nanson, J. D., Shi, Y., Sasaki, Y., Cunnea, K., et al. 2021. SARM1 er en metabolisk sensor, der aktiveres af et øget NMN/NAD(+)-forhold for at udløse aksondegeneration. Neuron. (2021) 109:1118-36.e11. doi: 10.1016/j.neuron.2021.02.009
[6] Jiang, Y., Liu, T., Lee, C. H., Chang, Q., Yang, J. og Zhang, Z. 2020. NAD+ -medieret selvhæmmende mekanisme for pro-neurodegenerativ Sarm1. Nature (2020) 588:658-63. doi: 10.1038/s41586-020-2862-z
Mennesker har lavet musik i titusinder af år. Men hvad sker der i din hjerne, når du lytter til dit yndlingsband eller din yndlingsmusiker? I denne artikel følger du lydens rejse fra ørerne til hjernen, hvor forskellige områder arbejder sammen, mens du lytter til musik. Musik involverer mange hjernefunktioner, såsom lydbehandling, hukommelse, følelser og bevægelse. Du vil også opdage, at hjernen kan lære at genkende velkendte mønstre i musik, hvilket kan hjælpe med at forklare, hvorfor musik kan gøre os glade, triste eller endda ophidsede. Til sidst vil du udforske, hvad der sker i musikeres hjerner, når de spiller på deres instrumenter.
…Kunstig intelligens (AI) systemer bliver ofte rost for deres imponerende præstationer inden for en lang række opgaver. Men mange af disse succeser skjuler et fælles problem: AI tager ofte genveje. I stedet for virkelig at lære, hvordan man udfører en opgave, bemærker den måske bare enkle mønstre i de eksempler, den har fået. For eksempel kan en AI, der er trænet til at genkende dyr på fotos, stole på baggrunden i stedet for selve dyret. Nogle gange kan disse genveje føre til alvorlige fejl, såsom en diagnose fr , der er baseret på hospitalsmærker i stedet for patientdata. Disse fejl opstår selv i avancerede systemer, der er trænet på millioner af eksempler. At forstå, hvordan og hvorfor AI tager genveje, kan hjælpe forskere med at designe bedre træningsmetoder og undgå skjulte fejl. For at gøre AI mere sikker og pålidelig skal vi hjælpe den med at udvikle en reel forståelse af opgaven – ikke bare gætte ud fra mønstre, der har fungeret tidligere.
…Er du nogensinde faldet og slået hovedet, mens du legede? Følte du dig lidt svimmel og havde ondt i hovedet? Hvis ja, kan du have fået en hjernerystelse! Hjernerystelser kan ske hvor som helst. De kan ske under sport, når du leger med dine venner eller endda når du cykler med dine forældre. Det kan være svært at vide, om du har fået en hjernerystelse. Mange børn og forældre er ikke sikre på, hvad de skal gøre, hvis nogen får en hjernerystelse. Læger og forskere ved, at det hjælper dig med at komme dig hurtigere, hvis du gør det rigtige efter en hjernerystelse. Denne artikel forklarer, hvad en hjernerystelse er. Den hjælper dig med at se, om du eller en ven har fået en hjernerystelse, og fortæller dig, hvad du skal gøre, hvis du nogensinde får en hjernerystelse.
…Hjertet er en meget vigtig muskel, der arbejder uafbrudt for at pumpe blod og levere vigtige næringsstoffer og ilt til alle dele af kroppen. Denne artikel ser på, hvordan hjertet fungerer normalt, og hvad der sker, når det fungerer unormalt, som det er tilfældet med en tilstand kaldet atrieflimren (AF). AF er en almindelig tilstand, der opstår, når hjertet slår uregelmæssigt og ude af takt. AF kan øge en persons risiko for at udvikle alvorlige problemer som hjertesvigt eller slagtilfælde. Denne artikel ser også på, hvordan AF kan diagnosticeres, hvad der forårsager AF, og de forskellige måder, det kan behandles på.
…