Forfattere

Sepsis er en livstruende reaktion på en infektion, hvor immunsystemet, som normalt hjælper med at bekæmpe infektioner, reagerer unormalt og kan få organer til at holde op med at fungere. Omkring 20 % af dødsfaldene på verdensplan skyldes sepsis – mere end nogen form for hjertesygdom eller kræft. Sepsis kan være svær for læger at genkende, fordi symptomerne i starten ligner mange andre medicinske tilstande, og det er svært at behandle, fordi de kropslige “funktionsfejl”, der forårsager sepsis, varierer fra patient til patient. For at kunne genkende sepsis tidligt og forstå forskellene mellem patienterne ser forskerne på mange dele af immunsystemet på én gang og indsamler masser af data om patienternes gener og proteiner. Computere bruges til at analysere dataene for at identificere unikke mønstre eller forbindelser. På den måde har forskerne identificeret unikke grupper af sepsispatienter, der adskiller sig i deres immunrespons. Denne viden kan hjælpe lægerne med at vælge den bedste behandling for hver enkelt person og måske endda hjælpe med at beskytte folk mod alvorlig COVID-19 eller fremtidige pandemier.
På et eller andet tidspunkt har du sikkert haft en infektion – måske blev et sår eller en hudafskrabning, du fik, da du legede udendørs, rød og hævet, eller måske havde du feber og hoste og fik konstateret influenza, lungebetændelse eller COVID-19. Du er måske kommet dig på egen hånd eller har fået ordineret medicin til at behandle infektionen, men chancerne er store for, at du er kommet dig uden de store problemer – takket være dit immunsystem. Normalt fungerer immunsystemet som et veltrænet forsvarshold, der identificerer og angriber skadelige indtrængere og hjælper vores kroppe med at komme sig. Men nogle gange kan det gå galt.
Når nogle mennesker får alvorlige infektioner, især ældre mennesker eller dem, der allerede er syge eller svage, kan immunsystemet blive dysreguleret. I disse tilfælde reagerer immunsystemet ikke på infektionen, som det burde – det kan f.eks. overreagere og skade sunde dele af kroppen eller ikke reagere kraftigt nok, så bakterierne lettere kan sprede sig. Dysregulering af immunsystemet kan føre til en meget alvorlig medicinsk tilstand kaldet sepsis-En unormal, livstruende reaktion på en infektion, som påvirker hele kroppen. Tænk på det som en brand, der bryder ud i ét rum, men som derefter hurtigt spreder sig til hele huset. I de værste tilfælde kan sepsis få vitale organer som hjerte, lunger og nyrer til at holde op med at fungere ordentligt, hvilket fører til døden.
Det vil måske overraske dig at høre, at sepsis er en af de største dødsårsager på verdensplan. Faktisk forårsager sepsis næsten 1 ud af 5 dødsfald hvert år – mere end nogen form for hjertesygdom eller kræft! Alene i 2017 dræbte sepsis omkring 11 millioner mennesker [1]. Mange mennesker er ikke klar over, hvor almindelig og dødelig sepsis er, bl.a. fordi den ikke altid angives som dødsårsag – ofte er den “skjult” bag andre infektioner eller sygdomme, som personen måske har lidt af. COVID-19-pandemien understregede dette problem, da de fleste dødsfald forårsaget af alvorlig COVID faktisk skyldtes sepsis, hvor virussen udløste en dysreguleret immunrespons [2].
I øjeblikket omfatter behandling af sepsis medicin til at bekæmpe den underliggende infektion og støttende behandling for at holde organerne i gang – men der er ingen behandlinger til at afhjælpe den dysfunktion i immunsystemet, der forårsager sepsis i første omgang. Sepsisbehandlinger virker måske hos nogle patienter, men ikke hos andre, og selv med de nuværende behandlinger dør >22 % af de mennesker, der indlægges med sepsis [1].
En af de ting, der gør sepsis så dødbringende, er, at det ofte er svært for lægerne at vide, hvornår patienterne har det. De tidlige symptomer på sepsis kan ligne symptomerne på mange andre almindelige sundhedsproblemer – for eksempel unormal kropstemperatur, blodtryk, vejrtrækningsfrekvens og hjerterytme – hvilket gør det vanskeligt at stille en tidlig diagnose [3]. En anden ting, der gør det svært at diagnosticere sepsis, er, at symptomerne kan være forskellige fra patient til patient, så der findes ikke en liste over symptomer, som lægerne kan “tjekke af” for at bekræfte, at sepsis er problemet. Jo længere tid det tager en læge at diagnosticere sepsis, jo mere syg bliver patienten, og jo sværere er sepsis at behandle. Variationen er også med til at forklare, hvorfor nogle behandlinger måske ikke virker for alle patienter.
Forskerne ved stadig ikke, hvorfor sepsis er så varierende. Variationen kan skyldes patientfaktorer som alder, køn, gener, andre sygdomme, som patienten måtte have, og de typer medicin, de tager. Variationen kan også skyldes faktorer, der er specifikke for infektionen, f.eks. hvilken type organisme, der forårsagede den (f.eks. bakterier eller virus), det oprindelige infektionssted (f.eks. lunger, urinveje eller hud), eller hvor længe patienten har haft sygdommen (figur 1).
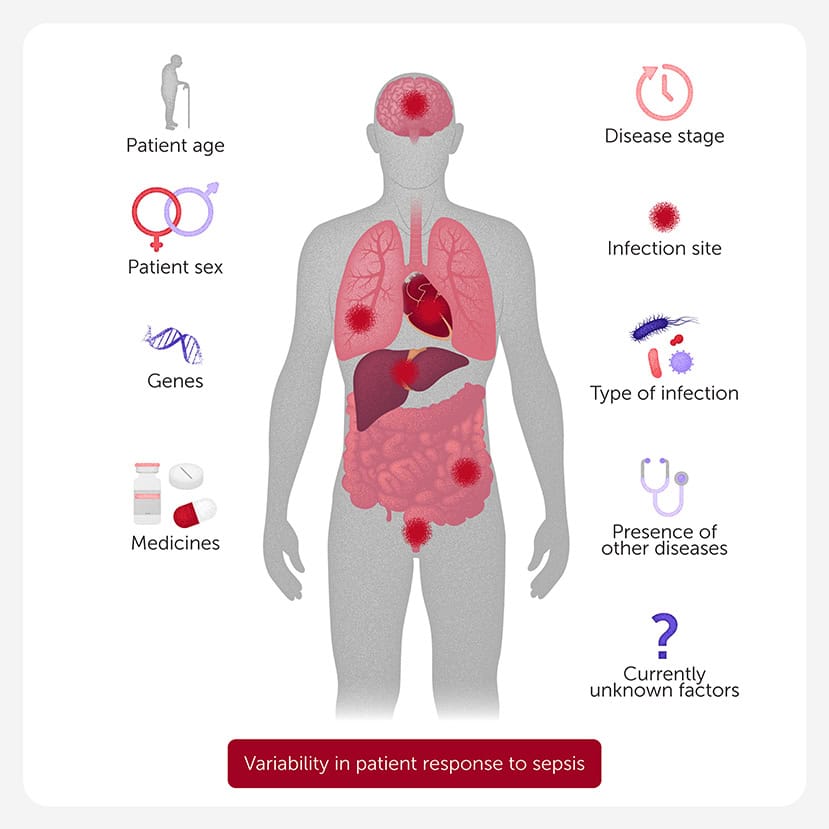
For at forbedre diagnosticering og behandling af sepsis er forskerne først nødt til at forstå, hvad der sker i de enkelte patienters immunsystem. Måske kan en forståelse af, hvordan immunsystemet bliver dysfunktionelt, hjælpe med at forklare, hvorfor sepsis-symptomer er så forskellige fra patient til patient.
Forestil dig, at du prøver at lægge et puslespil med 1.000 brikker. Hvordan ville du tackle denne udfordring – ville du “zoome ind” for at fokusere på de små detaljer i hver enkelt brik, eller “zoome ud” og se på det “store billede” på æsken? Sandsynligvis lidt af begge dele, ikke? Men uden det store billede ville det være meget sværere at lægge puslespillet.
Som et stort puslespil består immunsystemet af hundredvis af komponenter. Mange typer celler og proteiner arbejder sammen om at beskytte vores kroppe mod angribere. Den dysregulering, der opstår under sepsis, kan involvere mange af immunsystemets “puslespilsbrikker”, og det påvirker også andre kropslige systemer. At “zoome ind” for at undersøge, hvordan én type celle eller protein agerer under sepsis, kan give forskerne nogle vigtige oplysninger, men kun ved at “zoome ud” kan de se, hvordan alle brikkerne arbejder sammen, og hvordan den komplekse koordinering kan gå galt. Denne type “big picture”-tilgang, hvor matematisk analyse bruges til at hjælpe forskere med at forstå immunitet, kaldes systemimmunologi [4]. Men hvordan kan forskere helt præcist bruge systemimmunologi til at forstå sepsis?
En måde, hvorpå forskere har brugt systemimmunologi til at forstå det “store billede” af immunsystemet ved sepsis, er ved at se på, hvilke gener i immunsystemet der er aktive (tændte) hos sepsispatienter. Som du måske allerede ved, er gener cellulære instruktioner til fremstilling af proteiner – de molekyler, der er ansvarlige for næsten alt, hvad der sker i vores kroppe, fra opbygning af væv og organer til bekæmpelse af infektioner (figur 2A). Under sepsis bliver visse gener mere aktive end normalt, mens andre kan blive mindre aktive, hvilket påvirker, hvordan immunsystemet reagerer.
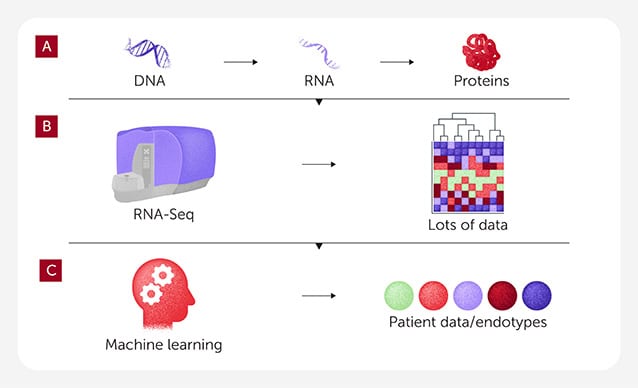
Forskere kan bruge effektive laboratorieteknikker, herunder en metode kaldet RNA-Seq for at undersøge, hvor aktive de enkelte gener er. I bund og grund “måler” de genaktiviteten i en patients celler ved at se på produktionen af RNA, som sker, når et gen aktiveres til at lave proteiner (figur 2B). Ved at se på, hvor aktive (eller inaktive) visse gener er hos sepsispatienter, kan forskerne begynde at forstå, hvordan immunsystemet er dysreguleret ved sepsis, og hvordan det opfører sig forskelligt fra person til person.
Da forskere brugte RNA-Seq til at studere immunceller fra hundredvis af mennesker med sepsis, stod de over for en enorm mængde data – mere end de overhovedet kunne analysere uden hjælp fra computere. Så de henvendte sig til machine learning En type kunstig intelligens, der kan gennemgå store mængder data for at finde skjulte mønstre (figur 2C). Maskinlæring identificerede almindelige gener med ændret aktivitet, hvilket muliggjorde en tidlig diagnose. Forskerne opdagede også variationer mellem patienter og identificerede fem hovedtyper af sepsis, som de kaldte endotyper. Hver endotype repræsenterer et unikt immunsystemrespons med sit eget specifikke sæt af 200 gener, som enten er mere eller mindre aktive end normalt, hvilket resulterer i forskellige symptomer (figur 3) [5]. For eksempel indikerer RNA-Seq, at patienter med én endotype har en type sepsis, hvor immunsystemet er overaktivt, hvilket fører til overdreven inflammation, mens immunsystemet hos en anden endotype måske er undertrykt (ikke aktivt nok) og kæmper for at bekæmpe infektionen.
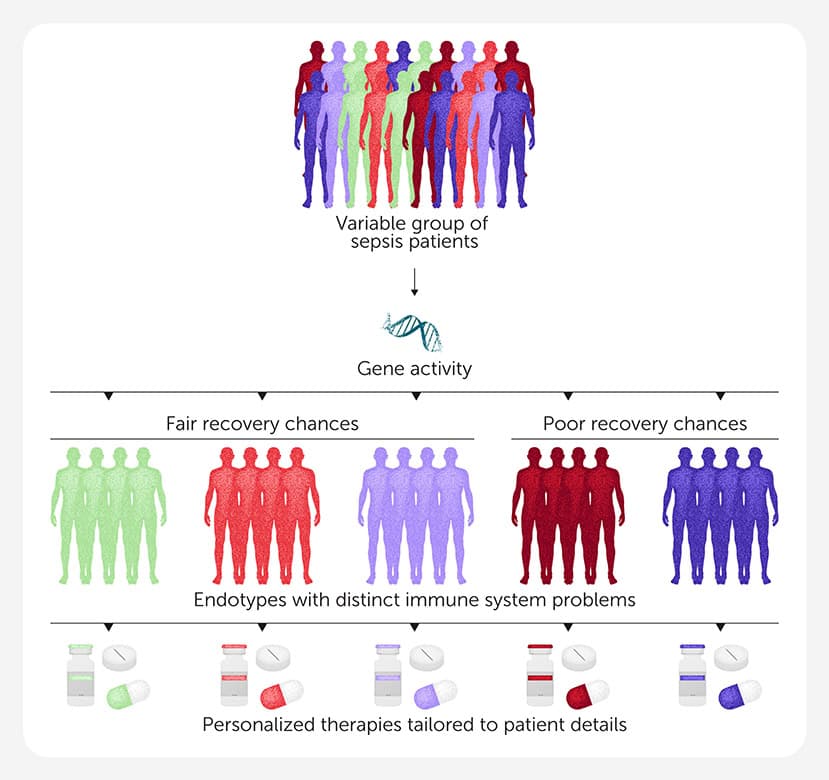
Opdagelsen af sepsis-endotyper er spændende, fordi de kan opdages meget tidligt – tidligere end læger normalt kan diagnosticere sepsis. Som nævnt gælder det, at jo tidligere patienterne diagnosticeres, jo bedre er deres chancer for at komme sig. Endotyper kan også hjælpe med at forklare, hvorfor nogle patienter reagerer på en bestemt behandling, mens andre ikke gør. Dette åbner døren til personlig medicin-En tilgang, hvor lægerne skræddersyr behandlinger til de specifikke detaljer i hver enkelt patient i stedet for at forlade sig på en løsning, der passer til alle. Baseret på en patients genaktivitet vil lægerne måske snart kunne diagnosticere den specifikke endotype af sepsis, som en patient har, og give den behandling, der vil være mest effektiv for deres særlige tilstand – et stort skridt fremad!
Sepsis er ikke bare forskellig fra patient til patient – den ændrer sig også over tid inden for den samme patient. Det betyder, at immunsystemet kan opføre sig forskelligt på forskellige stadier, efterhånden som sepsis skrider frem. I begyndelsen kan det være hyperaktivt og forårsage overdreven inflammation, men senere kan det blive undertrykt, hvilket sætter patienten i fare for yderligere infektioner. Disse skift i immunresponser over tid er en anden faktor, der i øjeblikket gør sepsis vanskelig at behandle. Ved at bruge RNA-Seq kan forskerne spore, hvordan immunsystemets genaktivering ændrer sig over tid hos den enkelte patient. Sådanne oplysninger kan føre til stadiespecifikke behandlinger – behandlinger, der ikke kun er skræddersyet til den endotype af sepsis, som en patient har, men også til, om de er i den tidlige, midterste eller sene fase af sygdommen. Mere præcise og effektive behandlinger kan forbedre patienternes chancer for at komme sig.
At forstå, hvad der forårsager sepsis, og hvordan man behandler det, kan også hjælpe lægerne med at håndtere alvorlige tilfælde af virusinfektioner som COVID-19. Mange forskere mener nu, at fremtidige pandemier også kan involvere en eller anden form for sepsis, uanset hvilken virus eller bakterie der er involveret. Det betyder, at det kan være et vigtigt mål at udvikle behandlinger, der er rettet mod en dysfunktionel immunrespons snarere end den specifikke bakterie. Hvis forskere kan finde måder at håndtere den immundysfunktion, der ses ved sepsis, kan de redde liv i fremtidige pandemier – selv før specifikke vacciner eller behandlinger mod infektionen er tilgængelige.
I sidste ende handler studiet af sepsis om mere end at forstå en enkelt sygdom – det handler om at løse et puslespil, der kan være med til at forbedre sundheden for millioner af mennesker over hele verden [6.] Ved at se på det store billede og lære, hvordan immunsystemet reagerer på infektioner, redder forskerne ikke kun liv i dag, men forbereder sig også på morgendagens udfordringer.
Immunsystemet: Et komplekst netværk af organer, celler, gener og proteiner, der forsvarer kroppen mod infektioner; sygdomme opstår, når det svigter eller reagerer uhensigtsmæssigt.
Dysreguleret: Når genaktiviteten ændres, så immunsystemet reagerer forkert – enten overreagerer, underreagerer eller angriber kroppen selv, hvilket fører til forskellige sygdomme og helbredsproblemer.
Sepsis: En unormal, livstruende reaktion på infektion, der fører til (multi)organdysfunktion og -svigt; skyldes et dysreguleret immunsystem.
Systemimmunologi: Et felt, der studerer alle dele af immunsystemet sammen, f.eks. gener og proteiner, for at se, hvordan de fungerer og interagerer. Forskere bruger computerværktøjer til at forstå disse komplekse forbindelser.
RNA-Seq: En metode til at omdanne RNA til DNA og derefter sekventere det for at bestemme aktiviteten af hvert gen i kroppen. Kaldes også transkriptom-sekventering.
Maskinel indlæring: En type AI, hvor computere bruger data og gentagne beregninger til at efterligne menneskelig tænkning, forbedre løsninger over tid og håndtere meget mere information, end mennesker kan.
Endotyper: Grupper af patienter med lignende underliggende årsager til en sygdom. Komplekse sygdomme som sepsis, kræft og astma har forskellige endotyper, der påvirker progression, sværhedsgrad og behandlingseffektivitet.
Personlig medicin: Anerkendelse og brug af en persons specifikke karakteristika til at styre beslutninger om forebyggelse, diagnose og behandling af sygdomme.
[1] Rudd, K. E., Johnson, S. C., Agesa, K. M., Shackelford, K. A., Tsoi, D., Kievlan, D. R., et al. 2020. Global, regional og national sepsisforekomst og -dødelighed, 1990-2017: analyse til den globale sygdomsbyrdeundersøgelse. Lancet. 395:200-11. doi: 10.1016/S0140-6736(19)32989-7
[2] Vincent, J. L. 2021. COVID-19: Det hele handler om sepsis. Future Microbiol. 16:131-3. doi: 10.2217/fmb-2020-0312
[3] Vincent, J.-L. 2016. Den kliniske udfordring ved identifikation og overvågning af sepsis. PLoS Med. 13:e1002022. doi: 10.1371/journal.pmed.1002022
[4] Forlin, R., James, A., Brodin, P. 2023. At gøre menneskets immunsystem mere fortolkeligt gennem systemimmunologi. Trends Immunol. 44:577-584. doi: 10.1016/j.it.2023.06.005
[5] Baghela, A., Pena, O. M., Lee, A. H., Baquir, B., Falsafi, R., An, A., et al. 2022. Forudsigelse af sværhedsgraden af sepsis ved første kliniske præsentation: endotypernes og de mekanistiske signaturers rolle. eBioMedicine. 75:103776. doi: 10.1016/j.ebiom.2021.103776
[6] Maslove, D. M., Tang, B., Shankar-Hari, M., Lawler, P. R., Angus, D. C., Baillie, J. K., et al. 2022. Omdefinering af kritisk sygdom. Nat. Med. 28:1141-1148. doi: 10.1038/s41591-022-01843-x
Mennesker har lavet musik i titusinder af år. Men hvad sker der i din hjerne, når du lytter til dit yndlingsband eller din yndlingsmusiker? I denne artikel følger du lydens rejse fra ørerne til hjernen, hvor forskellige områder arbejder sammen, mens du lytter til musik. Musik involverer mange hjernefunktioner, såsom lydbehandling, hukommelse, følelser og bevægelse. Du vil også opdage, at hjernen kan lære at genkende velkendte mønstre i musik, hvilket kan hjælpe med at forklare, hvorfor musik kan gøre os glade, triste eller endda ophidsede. Til sidst vil du udforske, hvad der sker i musikeres hjerner, når de spiller på deres instrumenter.
…Kunstig intelligens (AI) systemer bliver ofte rost for deres imponerende præstationer inden for en lang række opgaver. Men mange af disse succeser skjuler et fælles problem: AI tager ofte genveje. I stedet for virkelig at lære, hvordan man udfører en opgave, bemærker den måske bare enkle mønstre i de eksempler, den har fået. For eksempel kan en AI, der er trænet til at genkende dyr på fotos, stole på baggrunden i stedet for selve dyret. Nogle gange kan disse genveje føre til alvorlige fejl, såsom en diagnose fr , der er baseret på hospitalsmærker i stedet for patientdata. Disse fejl opstår selv i avancerede systemer, der er trænet på millioner af eksempler. At forstå, hvordan og hvorfor AI tager genveje, kan hjælpe forskere med at designe bedre træningsmetoder og undgå skjulte fejl. For at gøre AI mere sikker og pålidelig skal vi hjælpe den med at udvikle en reel forståelse af opgaven – ikke bare gætte ud fra mønstre, der har fungeret tidligere.
…Er du nogensinde faldet og slået hovedet, mens du legede? Følte du dig lidt svimmel og havde ondt i hovedet? Hvis ja, kan du have fået en hjernerystelse! Hjernerystelser kan ske hvor som helst. De kan ske under sport, når du leger med dine venner eller endda når du cykler med dine forældre. Det kan være svært at vide, om du har fået en hjernerystelse. Mange børn og forældre er ikke sikre på, hvad de skal gøre, hvis nogen får en hjernerystelse. Læger og forskere ved, at det hjælper dig med at komme dig hurtigere, hvis du gør det rigtige efter en hjernerystelse. Denne artikel forklarer, hvad en hjernerystelse er. Den hjælper dig med at se, om du eller en ven har fået en hjernerystelse, og fortæller dig, hvad du skal gøre, hvis du nogensinde får en hjernerystelse.
…Hjertet er en meget vigtig muskel, der arbejder uafbrudt for at pumpe blod og levere vigtige næringsstoffer og ilt til alle dele af kroppen. Denne artikel ser på, hvordan hjertet fungerer normalt, og hvad der sker, når det fungerer unormalt, som det er tilfældet med en tilstand kaldet atrieflimren (AF). AF er en almindelig tilstand, der opstår, når hjertet slår uregelmæssigt og ude af takt. AF kan øge en persons risiko for at udvikle alvorlige problemer som hjertesvigt eller slagtilfælde. Denne artikel ser også på, hvordan AF kan diagnosticeres, hvad der forårsager AF, og de forskellige måder, det kan behandles på.
…